Die elementare Ordnung der Welt
118 Elemente sind Naturwissenschaftlern bis heute bekannt – einige könnten auf der Erde bald nicht mehr zu finden sein.
„
 Aus solchen Wismut-Kristallen wird in Bismut isoliert. Auch das für Legierungen gebrauchten Element gehört zu den 44, die in…
Aus solchen Wismut-Kristallen wird in Bismut isoliert. Auch das für Legierungen gebrauchten Element gehört zu den 44, die in…
Den Stars der Nerd-Serie „Big Bang Theory“ dient es als dekorativer Duschvorhang, Lehrer hingegen nutzen es im Chemieunterricht nicht nur als Wandschmuck: Das Periodensystem der Elemente (PSE) hat dieses Jahr 150-jähriges Jubiläum. Aufgrund seines „Stellenwerts für Wissenschaft und Wirtschaft“ widmen die Vereinten Nationen der Tabelle, die alle Stoffe des Universums ordnet, ein „Weltjahr“. In Paris wird dafür am 29. Januar eigens das „internationale Jahr des Periodensystems der chemischen Elemente“ verkündet.
Alle 118 Elemente, die bisher nachgewiesen wurden, ordnet das PSE nach Anzahl der Protonen. Es ist aber längst nicht nur bloßes Hilfsmittel in der Chemie, sondern stellt auch dar „woraus wir und alles was uns umgibt aufgebaut ist – also letzten Endes die gesamte Materie“, sagt Christian Müller, Professor für Anorganische Chemie an der Freien Universität Berlin.
Zwei Forscher, ein Gedanke
Auf die Idee, Ordnung ins chemische Durcheinander zu bringen, kamen vor 150 Jahren gleich zwei Forscher, unabhängig voneinander: der Russe Dmitri Mendelejew und wenige Monate später der Deutsche Lothar Meyer, „der leider oft vergessen wird“. sagt Müller. Sie entwickelten eine Tabelle, in die sie die bis dahin bekannten Elemente anhand ihrer Eigenschaften einsortierten. Damit wurden Prognosen über noch nicht entdeckte Stoffe einfacher – wo die Tabelle eine Lücke aufwies, musste ein Element existieren, das noch gefunden werden musste.
Die einzelnen Elemente im PSE sind in Zeilen (Perioden) und Spalten (Gruppen) angeordnet. Wobei „die Elemente mit ähnlichen Eigenschaften und gleicher Außenelektronenzahl untereinander angeordnet sind“, sagt Müller. Zu welcher Gruppe ein Element gehört, hilft bei der Vorhersage, ob und wie Reaktionen mit anderen Elementen möglich sind.
Außerdem enthält jedes Kästchen eine Vielzahl an Informationen, beispielsweise über den Aggregatzustand, die Dichte, und ob das Element radioaktiv ist oder nicht, und ist so eine wichtige Übersicht für verschiedenste naturwissenschaftliche Fragestellungen. Die Chemikerin, die für ein Experiment die Elektronegativität von Kupfer wissen muss, findet diese genauso, wie der Biologe die nötigen Information für das Ansetzen einer Nährlösung oder der Materialwissenschaftler für eine Legierung.
Von Wasserstoff bis Organesson
Oben links mit der Ordnungszahl eins steht heute wie damals das am einfachsten aufgebaute Element: Wasserstoff besitzt nur ein Elektron und ein Proton und ist deshalb für diverse quantenchemische Berechnungen das beste „Versuchselement“. Mit steigenden Zahlen werden die Elemente schwerer und komplexer: Sauerstoff beispielsweise besitzt die Ordnungszahl acht, Kohlenstoff, der Baustoff des Lebens, ist etwas leichter, steht zwei Plätze weiter links auf Platz sechs. Deutlich schwerer sind Iod (53), das man aus Desinfektionsmitteln kennt, und Metalle wie Gold (79) und Quecksilber (80). Manche Elemente sind weitgehend unbekannt: Yttium und Seaborgium etwa begegnen einem im Alltag eher selten. Das Element mit der bisher höchsten Ordnungszahl ist Organesson: als 118. Element komplettiert es die siebte Reihe.
Endliche Ressourcen
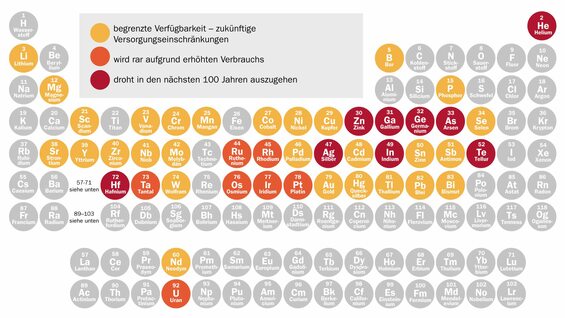
Noch kommen 94 der 118 bekannten Elemente natürlich vor, doch die Ressourcen auf der Erde sind endlich. Laut der „American Chemical Society“ wird es bei 44 von ihnen in den nächsten Jahren zu Versorgungseinschränkungen kommen. „Das ist im Moment vor allem auf die Handy-Produktion zurückzuführen“, sagt eine Sprecherin der Gesellschaft Deutscher Chemiker (GDCh). Denn betroffen sind neben Metallen wie Silber und Zink auch weniger bekannte Elemente wie Gallium, Hafnium und Indium. Diese Elemente kommen nur in sehr geringen Mengen auf der Erde vor, werden aber für Halbleiter- und Raumfahrttechnik sowie Touchscreens gebraucht. Da einerseits viele Menschen ihre alten Smartphones nicht entsorgten und das Recycling andererseits sehr aufwendig sei, gäbe es für viele dieser Elemente keinen Kreislauf, sodass immer weniger davon zur Verfügung stehen, sagt die GDCh-Sprecherin. Sogar Helium werde vermutlich in den nächsten „Jahren oder Jahrzehnten“ knapp.
Helium verhilft nicht nur Luftballons zum Fliegen
Das Edelgas leitet den Schall nicht nur schneller als Luft und sorgt so beim Einatmen für die bekannte Donald-Duck-Stimme, sondern hat auch eine Reihe technischer Anwendungen: Verflüssigt wird es dank seines sehr niedrigen Schmelzpunkts von 269 Grad Celsius oft als Kühlmittel verwendet, etwa für Supraleiter. Aufgrund geringer Dichte und Reaktionsträgheit eignet sich Helium auch für Luftschiffe und als Schutzgas. Problematisch dabei ist, dass Helium nicht in Verbindungen vorkommt, aus denen man es isolieren könnte, sondern nur als reines Gas. Als solches hat es sich über Millionen Jahre hinweg aus dem radioaktiven Zerfall von Thorium gebildet und im Erdinneren gesammelt. Von dort steigt es mit anderen Gasen im Gestein auf und wird bei der Erdgasförderung abgetrennt. Doch der Verbrauch übersteigt die Förderung im Moment massiv. Alternative Methoden wie die künstliche Herstellung durch Kernreaktionen oder die Isolation aus Luft sind sehr teuer und energieaufwendig.
An den Grenzen des Periodensystems
Ebenfalls teuer, energieaufwendig und kompliziert ist die Herstellung der Elemente mit der Ordnungszahl 95 und höher. Denn diese Elemente kommen auf der Erde nicht natürlich vor, sondern werden im Labor oder im Kernreaktor hergestellt. Das erste so produzierte Element war 1944 Americium, das inzwischen als Quelle ionisierender Strahlung genutzt wird. Schon bei den Elementen mit den Nummern 104 und 105 wurde klar, dass die Periodizität des Systems bei schweren künstlich hergestellten Elementen ihre Grenzen erreicht. Das liegt daran, dass sich ihre Elektronen nahezu mit Lichtgeschwindigkeit bewegen müssen und relativistische Effekte deshalb eine immer größere Rolle spielen. Die Elemente zeigen daher oft nicht mehr das Reaktionsverhalten und die Eigenschaften, welche man durch ihre Stellung im Periodensystem vermuten würde. Bei den aktuellsten Neuzugängen lassen sich die Eigenschaften aber ohnehin kaum noch messen: So existieren die neusten vier Elemente (Ordnungszahlen 113 bis 115), die erst im November 2016 ihre Namen und Abkürzungen bekamen, nur wenige Sekundenbruchteile. Diese superschweren Elemente werden erzeugt, indem Ionen leichterer Elemente mit sehr hoher Geschwindigkeit auf schwerere Elemente geschossen werden. Ihr Nachweis ist sehr aufwendig. An den folgenden Elementen 119 und 120 wird aktiv geforscht, unter anderem im GSI Helmholtzzentrum für Schwerionenforschung in Darmstadt. Bei welcher Ordnungszahl endgültig Schluss ist, ist unbekannt: Schätzungen gehen davon aus, dass insgesamt zwischen 126 und 173 Elemente möglich sind.
Start von Indiens erster Mondlandemission abgebrochen
Für den Start seiner ersten Mondlandemission hatte Indien sich ein historisches Datum ausg…






